Raimund Kalinowski
Unternehmensberatung
und Sachverständigenbüro
[Anm.:
(falls Sie auf diese Seite direkt durch einen link einer Suchmaschine
gekommen sein sollten), der Verfasser lädt Sie zum stöbern ein und freut sich über Rückmeldungen - bitte beachten Sie die Hinweise zum copyright unter Kontakt]
Systemvergleich
Entgasungen (Teil 1)- Karbonisierungen (Teil 2) Physikalische Grundlagen - vereinfacht dargestellt Im Physikunterricht werden gerne allerlei Taschenspielertricks vorgeführt und noch komplizierter, als die eigentlich sehr einfache Mengenlehre erklärt. Anders ist es nicht zu deuten, dass, sobald das Wort „Partialdruck“ in einer Besprechung fällt, einem Unverständnis umgibt. Ohne zu verstehen, das das Wort „Partialdruck“ etwas so einfaches, wie das unterschiedliche Obst in der Schale ausdrückt, ist es kaum möglich, die gängigen Entgasungen und Karbonisierungen zu unterscheiden. Stellen wir uns nun obige Obstschale vor. Wir entnehmen eine Birne von ganz unten - die Wahrscheinlichkeit, dass der Raum, den die Birne gerade ausfüllte, frei bleibt, ist äußerst gering - das andere Obst wird nachrücken und den gerade frei gewordenen Raum ausfüllen. Im Prinzip geschieht das gleiche mit Gasen. An der Erdoberfläche haben wir einen Luftdruck von etwa einem bar. Dieser Luftdruck wird durch die Erdanziehung und dem „Gewicht“ der Gase in der Atmosphäre erzeugt. Wenn man sich nun die Erde als Kugel vorstellt und das Gewicht der gesamten Atmosphäre durch die Oberfläche dieser Erdkugel teilt, wird man als Ergebnis ziemlich genau 1 kg pro cm² Erdkugeloberfläche erhalten. D.h. auf jeden Quadratzentimeter drückt eine Last von 1 kg. Wenn wir nun den Sauerstoff aus der Erdatmosphäre entfernen, würden die anderen, verbliebenen Gase den freigewordenen Raum ausfüllen. Die Gesamtmasse der Erdatmosphäre wäre nun um diese 21% des Luftsauerstoffs reduziert worden und die Last betrüge nicht mehr 1 kg sondern nur noch 0,79 kg pro Quadratcentimeter, dass heißt, der Druck hätte von 1 auf 0,79 bar abgenommen. So wie je nach Obst-Sorte und Größe der Schale eine verschieden große Anzahl von Obst in die Schale passt, so ist auch die Löslichkeit eines Gases in einer Flüssigkeit von der Gassorte, vom Vorhandensein weiterer Gase und von der Flüssigkeit in der die Gase gelöst werden sollen, abhängig. Bei höherem Druck und geringeren Temperaturen lässt sich mehr Gas lösen. Bei der Wasserentgasung wird üblicherweise der verbliebene Sauerstoffgehalt gemessen. Diese Methode ist geeignet, wenn es primär um die Entfernung des Sauerstoffs geht. Falls entgast wird, um danach zu karbonisieren, sind auch andere gelöste Gase von Bedeutung. Die in Produktionsrichtung gesehen erste Wasserentgasung wird meist nicht als solche gesehen. Zur Entfernung des freien CO2 werden in der Wasseraufbereitung Rieseler eingesetzt. Rieseler sind im Prinzip stehende Tanks die mit Füllkörpern gefüllt sind. In der Wasseraufbereitung kommen meist Raschigringe aus Kunststoff (Polypropylen (PP)) als Füllkörper zum Einsatz. Raschigringe werden auch aus Glas oder aus Edelstahl angeboten. Für andere Einsatzzwecke wie z.B. zur Entfernung von Luft (-Sauerstoff) sind andere Füllkörper gebräuchlich, von einfachen Glasperlen bzw. Glaskugeln über Wilson Spiralen, Fenske Ringen (aufgeteilte Wilson Spiralen) bis hin zu diversen Sonderkonstruktionen. So benutzt ein Hersteller für die Wasserentgasung Füllkörper, die wie zerschnittene Platten von Plattenwärmeübertragern aussehen. Das Wasser wird oben auf die im Rieseler befindlichen Füllkörper geregnet. Das Wasser tropft nun von Füllkörper zu Füllkörper nach unten. Wenn man Sauerstoff entfernen will, wird nun von unten ein sauerstofffreies Gas meist CO2 eingeströmt. Es stellt sich ein Gleichgewicht ein, das CO2 nimmt auf dem Weg nach oben Luft aus dem Wasser auf und gleichzeitig wird CO2 im Wasser gelöst. Bei
einer thermischen Wasserentgasung wird das Wasser auf eine Temperatur
oberhalb des Siedepunktes (bei Entspannungsdruck) erwärmt.
Im heißen Wasser liegt die Luft nun nicht mehr gelöst
sondern in kleinen Bläschen vor. Beim entspannen des heißen
Wassers im Entgasungsgefäß, entsteht Wasserdampf, der
die kleinen Luftbläschen mitreißt. (Abb.1) Das Wasser
wird gleichzeitig entkeimt. Bei entsprechender Auslegung der Wärmerückgewinnung
sind die Kosten, wenn man den Doppelnutzen Entgasung und Entkeimung
sieht, noch vertretbar. Der Anfangssauerstoffgehalt oder die Zusammensetzung
des Wassers beeinflussen das Ergebnis der thermischen Wasserentgasung
nicht. Bestimmte Wasserinhaltsstoffe fallen beim Kochen aus. Dass
heißt, die thermische Wasserentgasung kann die Wasserzusammensetzung
evtl. verändern. Die Druckentgasung funktioniert ähnlich wie der Rieseler. Druckentgasungen werden auch für fertig ausgemischtes Getränk eingesetzt. Bei der Druckentgasung löst man nun ein Gas - meist CO2 - im zu entgasenden Wasser und entspannt das Wasser dann. Da sich der absolute Sauerstoffgehalt beim Lösen des CO2 nicht verändert hat, ist sein Gehalt im Verhältnis zum eingebrachten CO2 gesunken, so dass bei der Entspannung nicht nur das CO2 sondern auch andere im Wasser gelösten Gase im entsprechenden Verhältnis mit entfernt werden. Da CO2 im Wasser bzw. Getränk verbleibt, bietet sich die Druckentgasung mit CO2 insbesondere für karbonisierte Getränke an. Für andere Getränke könnte es sinnvoll sein, zum Beispiel Stickstoff statt CO2 einzusetzen. Bei
der Vakuumentgasung reduziert man den (Umgebungs-) Druck erheblich,
so dass sich entsprechend weniger Gase lösen können.
Wie bei der thermischen Entgasung, liegen die nicht mehr gelösten
Gase jetzt in sehr kleinen Bläschen vor. Wenn das Vakuum
groß genug ist, werden diese Gasbläschen entsprechend
größer. Bei entsprechend feiner Verdüsung des Wassers, haben die Gasbläschen eine Chance sich von der Oberfläche der Wassertröpfchen zu lösen. Durch die Zugabe eines anderen Gases (meist CO2 aber auch Stickstoff ist gebräuchlich) als sogenanntes „Strippinggas“ kann der Gastransport der Luft (des Sauerstoffs) unterstützt werden. Durch das zusätzliche Gas bilden sich größere Bläschen, die leichter abgeführt werden können. Jeder weiß, dass Champagner besonders fein perlt und karbonisierter Wein wesentlich größere Gasblasen bildet. Durch die Flaschengärung befindet sich im Champagner nahezu kein Sauerstoff, hingegen befindet sich im karbonisierten Wein eine entsprechende Menge an Sauerstoff, die hier als unerwünschtes „Strippinggas“ fungiert. Bei der Vakuum-Wasserentgasung kann als Strippinggas auch Wasserdampf eingesetzt werden. Dieser wird jedoch nicht zugeführt sondern wie bei der thermischen Entgasung durch das Verdampfen einer (sehr kleinen) Wassermenge, aus dem zu entgasenden Wasser heraus, erzeugt. Hierfür muss das Vakuum dem Siedepunkt des zu entgasenden Wassers entsprechen. Da die Vakuumpumpe wirtschaftlich sinnvoll, die anfallende Wasserdampfmenge nicht abführen kann, muss in diesem Falle vor der Vakuumpumpe ein Kondensator installiert werden. Da der Kondensator deutlich kälter sein muss als das zu entgasende Wasser, ist er an eine Kältemaschine anzuschließen. Falls bei dieser Verfahrensweise der Vakuumentgasung Flüssigkeitsringvakuumpumpen eingesetzt werden, ist darauf zu achten, dass das Betriebswasser der Vakuumpumpe ebenfalls deutlich unter die Temperatur des zu entgasenden Wassers gekühlt werden muss, da es sonst zu Kavitation kommt, die die Pumpe beschädigen kann. Da der Preis von Membranen kontinuierlich gesunken ist, werden Sie inzwischen als eine wirtschaftlich interessante Möglichkeit angeboten, Wasser zu entgasen. Hier wird die eine Seite einer gasdurchlässigen Membran mit einem sauerstofffreien Gas, meist CO2 oder Stickstoff, gespült und auf der anderen Seite das Wasser im Gegenstrom mit deutlich höherem Druck als auf der (Spül-)gasseite an der Membran entlang geführt. Wegen des großen Unterschiedes der Drücke strömt aus dem Wasser Sauerstoff und je nach Spülgas auch CO2 (bei Spülgas Stickstoff) oder Stickstoff (bei Spülgas CO2) in Richtung Spülgas. Der Spülgasstrom ist dem Wasserstrom entgegen gerichtet. Das Prinzip ähnelt einem Rieseler mit beliebig langer Behandlungszeit. Da die Gasseite im Unterdruck betrieben wird, ist die Aufnahme an Spülgas durch das Wasser zu vernachlässigen. Die katalytische Wasserentgasung wird großtechnisch z.B. in der Petrochemie genutzt; in Getränkebetrieben ist sie jedoch nur vereinzelt vertreten. Die katalytische Wasserentgasung kann äußerst wirtschaftlich sein, bietet aber auch einige Möglichkeiten, durch Fehlbedienungen sehr hohe Wartungskosten zu verursachen. Bei der katalytischen Wasserentgasung wird der Sauerstoffgehalt im Wasser gemessen und eine entsprechende Menge Wasserstoff hinzugegeben. Mit Hilfe eines Katalysators reagiert der Wasserstoff mit dem Sauerstoff und es bildet sich daraus Wasser. Alle anderen Inhaltsstoffe, inkl. der anderen gelösten Gase, wie z.B. Stickstoff, werden im Prinzip nicht verändert. Es ist rein technisch nicht möglich, diesen Vorgang molekülgenau zu steuern. Um Sauerstoffwerte im Bereich der Nachweisbarkeitsgrenze zu erzeugen, muss Wasserstoff im Überschuss zugegeben werden. Der nicht verbrauchte Wasserstoff verbleibt im Wasser. Wasserstoff ist relativ reaktionsfreudig. Es ist anzunehmen, dass er mit den Inhaltsstoffen des Wassers oder Getränks reagiert. Da die absolute Menge an Wasserstoff, die bei der Reaktion nicht verbraucht wird, relativ klein ist, konnte man bis jetzt weder eine Veränderung im Wasser / Getränk noch einen physiologischen Einfluss beim Menschen feststellen. Einige Entgasungen sind untrennbar in einen Mixer integriert. Bei der Druckentgasung ist dies in Verbindung mit der Karbonisierung eine wirtschaftliche Lösung. Insbesondere bei Großbetrieben ist hingegen ein Trend zu beobachten, zentrale Wasserentgasungen zu installieren und Funktionen sauber zu trennen, um auch verschiedenste Produkte problemlos herstellen zu können. Dieser Beitrag wird im kommenden Heft mit dem Kapitel Karbonisierung fortgesetzt. Systemvergleich Entgasungen (Teil 1)- Karbonisierungen
(Teil 2) Ist die Messung der Außentemperatur das geeignete Mittel, um die richtige Kleidung zu wählen oder die Heizungsanlage zu steuern? Was ist eigentlich Temperatur? Ende des 16ten Jahrhunderts hat vermutlich Galileo Galilei das Thermometer erfunden, obgleich in der Literatur häufig Cornelius Drebbel als Erfinder genannt wird. 1742 stellte der Schwede Anders Celsius ein Thermometer vor, bei dem die Messbedingungen klar definiert waren. Er legte fest, dass Wasser bei 0° und 760 mm Quecksilbersäule kocht und bei 100° beim gleichen Luftdruck gefriert. Die Teilung legte er durch gleichgroße Wärmeausdehnungsabschnitte des Quecksilbers fest. Erst viel später wurde übrigens die Temperaturskala umgedreht, so dass Wasser heute nicht bei 0° sondern bei 100° kocht. Wir messen also gar nicht Temperatur, sondern wir messen die Ausdehnung eines Metalls unter definierten Bedingungen und sagen dazu „Temperatur“. Die amerikanische Armee hat schon vor längerer Zeit festgestellt, dass die Leistungsfähigkeit und das Wohlbefinden eines Soldaten nur bedingt von der definierten Wärmeausdehnung eines Metalls abhängt. Es wurden Kriterien wie Wind und Luftfeuchte in eine Formel eingearbeitet, die inzwischen auch in Deutschland als „gefühlte Temperatur“ bezeichnet wird. Nun ist es beim Karbonisieren ähnlich. So wie man mit der Temperaturmessung eigentlich feststellen will, wie warm oder kalt es ist, möchte man mit der CO2-Gehaltsbestimmung eigentlich „den gefühlten Kribbeleindruck“ messen. Die CO2-Messung ist bis heute nicht klar definiert. Oder klarer ausgedrückt: Die CO2-Messung gibt es nicht. Meist wird ein Vergleichswert bestimmt. Große Firmen oder Verbände haben eigene Untersuchungsmethoden und Formeln aufgestellt. Messgerätehersteller versuchen ihre Messgeräte über Kalibrierkurven diesen ‚Vorgaben’ anzupassen. So, wie es relativ einfach ist, die Längenausdehnung zu messen und dies Temperatur zu nennen, wurden früher zur CO2-Gehalts-Bestimmung fast ausschließlich der Druck und die Temperatur unter möglichst definierten und reproduzierbaren Bedingungen gemessen. Über Tabellen, in denen meist Druck und Temperatur von Wasser bei der Sättigung mit CO2 unter gleichen Messbedingungen aufgelistet waren, wurde das CO2-Gehalts-Äquivalent bestimmt. Einflüsse wie der Luftdruck zum Zeitpunkt der Messung wurden meist nicht berücksichtigt. Andere Gase, wie z.B. die Luft im Flaschenhals, beeinflussen deutlich die Genauigkeit dieser Messung, weswegen nahezu alle Messvorschriften eine Druckentlastung nach einem Vorschütteln vorsehen. Auch heute noch ist die Schüttelmethode die gebräuchlichste Analysenmethode. Das, was als CO2-Gehalt mit dieser Analyse dokumentiert wird, weist jedoch mehr oder weniger deutlich vom wahren CO2-Gehalt im Getränk ab. In einigen dieser Formeln wird noch die Packungsgröße mit verrechnet. Der CO2-Gehalt wird üblicherweise in g/l oder in Ländern / Betrieben unter amerikanischem Einfluss in v/v angegeben. v/v bedeutet übrigens Volumen CO2 bei atmosphärischem Norm-Druck im Verhältnis zum Volumen des Getränks. Da CO2 eine Dichte von 1,98 kg/m³ hat, wird in der Praxis mit 1 v/v ˜ 2 g/l CO2 gerechnet. Die Angabe müsste nach dem zuvor gesagten, demnach nicht g/l oder v/v heißen sondern: „Eine Vergleichsflüssigkeit mit dem hier gemessenen Druck und der hier gemessenen Temperatur hätte bei Referenzbedingungen folgenden CO2-Gehalt“. Diese Bezeichnung hört sich jedoch etwas umständlich an. Neben der Schüttelmethode werden u.a.
auch Zusammengefasst bedeutet dies, die Einheit g/l oder v/v ist in der Praxis eine zwar gebräuchliche aber ungeeignete, da falsche Einheit. Zuckerhaltige Getränke und Getränke die noch bedeutende Mengen an Fremdgasen enthalten, lösen CO2 schlechter als zuckerfreie Getränke. Bestimmte Wasserinhaltsstoffe haben ebenfalls einen Einfluss auf die Lösungseigenschaften des CO2. Sulfatwässer unterscheiden sich hier z.B. deutlich von Hydrogencarbonatwässern. Insbesondere wenn man den getränkespezifischen CO2-Verbrauch ermittelt, wird man feststellen, dass die verwendeten Einheiten ziemlich unbrauchbar sind. In Ermangelung eines besseren, in der Praxis anwendbaren Verfahrens, wird man mit diesen Fehlern leben müssen. Prinzipiell werden 2 Arten von Karbonisierungen unterschieden. Behälterbasierte Systeme beruhen darauf das Getränk mit CO2 zu sättigen. Hierfür müssen Temperatur und Druck möglichst genau eingestellt werden. Da die Regelfehler bzw. Regelabweichungen absolut gesehen nahezu unabhängig von der absoluten Temperatur oder dem absoluten Druck sind, wird der Fehler bei steigendem CO2-Gehalt relativ gesehen, kleiner. Diese Anlagen werden insbesondere dort erfolgreich eingesetzt, wo hoch karbonisierte Getränke hergestellt werden. Häufig werden diese tankbasierten Karbonisierungen mit einer Druckentgasung kombiniert. Die konstruktive Gestaltung dieser Anlagen ist häufig sehr alt bzw. beruht auf solchen „bewährten“ Konstruktionen. Spül-, Reinigungs- und Produktwechselzeiten sind meist relativ lang, so dass sie wirtschaftlich sinnvoll entweder dort eingesetzt werden, wo Produktwechsel möglichst selten stattfinden oder wo die Umstellzeit aus anderen Gründen unbedeutend ist. Tankbasierte Karbonisierungen werden üblicherweise in einen Mixer integriert. Die andere Art der Karbonisierung beruht darauf, dass man die zu karbonisierende Getränkemenge und die dafür notwendige Menge CO2 möglichst genau erfasst, miteinander mischt und das CO2 dann vollständig im Getränk löst. Diese Karbonisierungen können als Einzelmaschinen ausgeführt werden. Der theoretische Vorteil besteht darin, dass der CO2-Gehalt weitgehend unabhängig von den Betriebsbedingungen in sehr weiten Bereichen sehr genau eingestellt werden kann. D.h. auch sehr schwach karbonisierte Getränke können mit der selben relativen Genauigkeit wie hochkarbonisierte Getränke hergestellt werden. Ebenso ist es möglich mehrere oder andere Gase als CO2 wie z.B. Stickstoff zu lösen. Es ist möglich diese Karbonisierungen als Inline-Karbonisierungen auszuführen, die sich reinigungstechnisch wie ein Stück Rohr verhalten. Um das eingebrachte CO2 vollständig zu lösen, muss die Oberfläche der Gasblasen groß, d.h. die Gasblasen selbst müssen möglichst klein sein. Der Betriebsdruck liegt oberhalb des Sättigungsdruckes, je höher der Betriebsdruck ist, desto leichter kann das CO2 gelöst werden. Möglichst lange Lösezeiten sind für das Lösen vorteilhaft, zehren aber an den Vorteilen, wie der kompakten Bauweise und der einfachen, schnellen Reinigungsfähigkeit. In
der Praxis hat sich gezeigt, dass Systeme mit Düsen Die Investitionskosten von behälterbasierten Systemen steigen nahezu proportional mit der Durchflussleistung an. Da der apparative und der Steuerungsaufwand der Inline-Karbonisierungen kaum von der Anlagenleistung abhängt, sind Anlagen kleiner Leistung teuer und der Anschaffungspreis sinkt relativ mit steigender Anlagenleistung. Ein nicht zu unterschätzender Vorteil der Inline-Karbonisierungen ist, dass das Gas zur Erzeugung des Kopfraumdrucks im Puffertank frei gewählt werden kann. So kann z.B. Druckluft oder Stickstoff (aus vor Ort Anlagen) eingesetzt werden, wodurch der CO2-Verbrauch und die damit verbundenen Kosten drastisch reduziert werden können. Obwohl
wir die Längenausdehnung eines Metalls zu Rate ziehen, um
zu entscheiden ob wir die Heizung einschalten sollten oder nicht,
so helfen uns doch all diese unzulänglichen Messwerte, um
z.B. einen für den Kunden qualitativ immer gleichen Zungenkribbeleindruck
zu produzieren sofern wir die Grenzen der heute üblichen
Systeme erkennen und akzeptieren. |
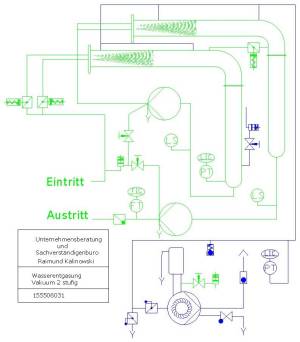
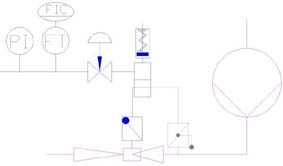 ,
statischen Mischern
,
statischen Mischern 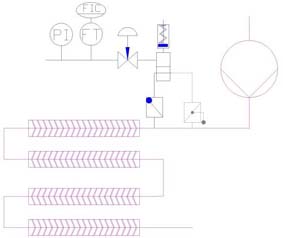 oder
Gasabscheidern mit Umwälzleitung
oder
Gasabscheidern mit Umwälzleitung 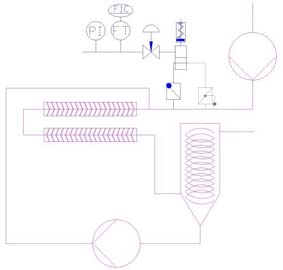 gleichgute
Ergebnisse erzielen können, sofern sie entsprechend „sauber“
konstruiert wurden. Neben den eingesetzten Mess- und Regelgeräten
entscheidet insbesondere die Regelphilosophie über das Ergebnis.
Eine einfache Proportionalregelung wird nur befriedigende Ergebnisse
liefern, wenn sich die Betriebsbedingungen wie Durchfluss, Temperatur
und Druck möglichst wenig ändern. Nicht das Konstruktionsprinzip
sondern die technische Umsetzung entscheidet über das Ergebnis.
gleichgute
Ergebnisse erzielen können, sofern sie entsprechend „sauber“
konstruiert wurden. Neben den eingesetzten Mess- und Regelgeräten
entscheidet insbesondere die Regelphilosophie über das Ergebnis.
Eine einfache Proportionalregelung wird nur befriedigende Ergebnisse
liefern, wenn sich die Betriebsbedingungen wie Durchfluss, Temperatur
und Druck möglichst wenig ändern. Nicht das Konstruktionsprinzip
sondern die technische Umsetzung entscheidet über das Ergebnis.